Administración de Biden anuncia cuándo suavizará restricciones de viaje y qué exigirá a viajeros

- La Administración del presidente Joe Biden anunció cambios en la restricción de viaje por la pandemia.
- EEUU informó cuándo comenzará a aplicar nuevas reglas y qué se les exigirá a los viajeros.
- Las restricciones de viaje a EEUU se han mantenido por meses debido a la crisis desatada por el coronavirus.
Estados Unidos suavizará algunas restricciones de viaje a partir de noviembre, cuando solicitará a todos los extranjeros que visiten el país que estén completamente vacunados contra el Covid-19, se anunció este lunes 20 de septiembre.
Todos los extranjeros que viajen a Estados Unidos deberán mostrar un comprobante de vacunación antes de abordar y una prueba negativa realizada dentro de los tres días previos al vuelo, informó el coordinador de Covid-19 de la Casa Blanca, Jeff Zients, quien anunció la nueva política, según reportó la agencia de noticias AP.
EEUU suavizará restricciones de viaje

Por otro lado, el gobierno del presidente Joe Biden también endurecerá las reglas para los estadounidenses quienes no se han vacunado, ya que deberán examinarse un día antes de salir de Estados Unidos, y lo mismo al regresar. Además, no se requerirá que los pasajeros completamente vacunados se pongan en cuarentena.
La nueva política reemplaza a las anunciadas primero por el gobierno de Donald Trump el año pasado y endurecidas luego por Biden, según las cuales quedaba restringida la entrada al país de los no ciudadanos que en los 14 días previos hayan estado en el Reino Unido, la Unión Europea, China, India, Irán, la República de Irlanda, Brasil y Sudáfrica.
Nuevas reglas sobre restricciones de viaje a EEUU

“Esta política depende de cada individuo y no de cada país, así que es una estrategia más sólida”, afirmó Zients. Además, los Centros para el Control y la Prevención de Enfermedades (CDC por sus siglas en inglés) le pedirán a las aerolíneas recaudar datos de los contactos de los pasajeros internacionales, a fin de facilitar el seguimiento de personas próximas en caso necesario, agregó.
No quedaba claro de inmediato cuáles vacunas serán aceptadas por Estados Unidos, o si el gobierno aceptará las que no se han aprobado en el país. El coordinador de Covid-19 de la Casa Blanca, Jeff Zients, declaró que esa decisión estará en manos de los CDC.
La nueva política sobre restricciones de viaje arranca en noviembre
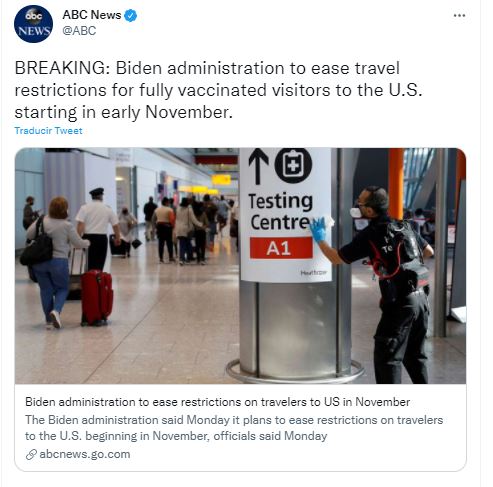
La nueva política entrará en vigencia a inicios de noviembre, con lo cual las aerolíneas y otras empresas de viajes tienen tiempo para implementar los nuevos requerimientos, indicó Zients, de acuerdo con el reporte de la agencia de noticias AP.
ABC News, NBC News, entre otros medios, también han reportado el anuncio de la Administración de Biden para suavizar las restricciones de viaje, vía aérea, a partir de noviembre, cuando se pondría fin a la separación de algunas familias desde marzo de 2020 debido a la pandemia.
Beneficio para viajeros en lista de países restringidos por Covid-19

Según ABC News, el anuncio se produce justo cuando el presidente Joe Biden se prepara para dirigirse a la Asamblea General de las Naciones Unidas en Nueva York este lunes y un día antes de reunirse en la Casa Blanca con el primer ministro del Reino Unido, Boris Johnson.
Las nuevas reglas aliviarán las restricciones de viaje que limitaron la entrada a Estados Unidos en muchos casos para los no ciudadanos que habían estado recientemente en 33 países, incluidas muchas naciones europeas y el Reino Unido, independientemente del estatus de vacunación. Pero para los viajeros fuera de esos países, el nuevo sistema establecerá requisitos más estrictos que podrían ser una barrera para quienes viven en países donde las vacunas escasean, reseñó NBC News.
Pfizer dice que su vacuna contra el COVID-19 funciona en niños de 5 a 11 años

La vacuna de Pfizer contra el COVID-19 funciona en niños entre 5 y 11 años, según anunció el lunes la compañía, que pedirá pronto la autorización en Estados Unidos para esa franja de edad, un paso clave para iniciar las vacunaciones en niños pequeños, reseñó The Associated Press.
La vacuna fabricada por Pfizer y su socio alemán BioNTech ya está disponible en Estados Unidos para personas de 12 años en adelante. Pero ahora que los niños han vuelto a la escuela y la contagiosa variante delta del virus ha causado un gran aumento de los contagios pediátricos, muchas familias esperan con ansiedad la oportunidad de vacunar a sus hijos más pequeños.
Vacuna Pfizer funciona en niños entre 5 y 11 años

La farmacéutica probó una dosis mucho menor para los niños de ese tramo de edad, un tercio de las dosis administradas hasta ahora. Sin embargo, tras la segunda dosis, los niños de entre 5 y 11 años mostraron niveles de anticuerpos para combatir al coronavirus tan fuertes como los de adolescentes y adultos jóvenes, indicó a The Associated Press el doctor Bill Gruber, vicepresidente senior de Pfizer.
La dosis reducida también se mostró segura, con efectos secundarios temporales -como molestias en el brazo, fiebre o dolor- similares o menores a los de los adolescentes, señaló. “Creo que de verdad dimos con el punto justo”, dijo Gruber, que también es pediatra.
Pfizer tiene previsto solicitar la aprobación de la FDA este mes
Las firmas tienen previsto solicitar este mes a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA por sus siglas en inglés) el uso de emergencia dela vacuna en esa franja de edad. Después se enviarían solicitudes a las autoridades reguladoras europea y británica.
El jefe de la FDA, el doctor Peter Marks, dijo a AP este mes que una vez Pfizer entregara los resultados de sus ensayos, su agencia estudiaría los datos “esperamos que en cuestión de semanas” para determinar si los fármacos eran seguros y efectivos para niños pequeños.
Otros países comenzaron la vacunación
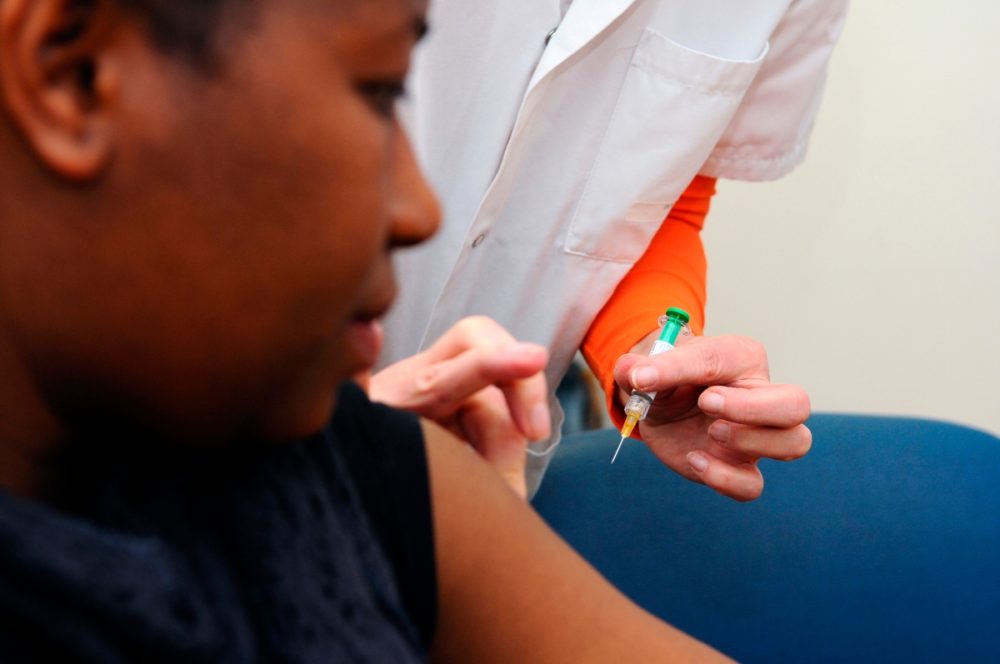
Muchos países occidentales han limitado las vacunaciones por ahora a partir de los 12 años hasta tener datos sobre cuál es la dosis correcta y su seguridad en pacientes más jóvenes. Sin embargo, Cuba empezó a inmunizar la semana pasada a niños a partir de dos años con su vacuna local, y las autoridades chinas han autorizado el empleo de dos de sus marcas a partir de 3 años.
Aunque los niños corren menos peligro de enfermar de gravedad o morir por COVID-19 que pacientes mayores, más de 5 millones de niños han dado positivo desde el inicio de la pandemia en Estados Unidos y al menos 460 han muerto, según la Academia Estadounidense de Pediatría. Los casos en niños han subido de forma drástica conforme la variante delta se extendía por el país.
Casos en niños han aumentado debido a variante delta
“Siento una gran sensación de urgencia” en ofrecer la vacuna para niños menores de 12 años, dijo Gruber. “Hay una demanda acumulada de los padres de poder devolver a sus hijos a una vida normal”, agregó, de acuerdo con el reporte del referido medio.
Pfizer dijo haber estudiado la dosis más baja en 2.268 alumnos de preescolar y primaria. La FDA requería un estudio inmune que mostrara que los niños pequeños desarrollaban respuestas inmunes que ya se han demostrado como protectoras en adolescentes y adultos. Eso fue lo que presentó Pfizer el lunes, y no una publicación científica.
Se desconocen todos los efectos secundarios
El estudio sigue en marcha, y todavía no se han producido suficientes casos de COVID-19 para comparar las cifras entre los vacunados y los que recibieron un placebo, algo que podría ofrecer más información. El estudio no es lo bastante grande para detectar efectos secundarios extremadamente raros, como la inflamación de corazón identificada en ocasiones tras la segunda dosis, especialmente en varones jóvenes.
Marks, el responsable de la FDA, señaló que los estudios pediátricos debían ser lo bastante grandes como para descartar riesgos mayores para los niños pequeños. Gruber dijo que una vez se haya autorizado el uso del fármaco en niños pequeños, los vacunados serán supervisados de forma meticulosa como otros pacientes para identificar riesgos poco frecuentes. Para mayor información visita esta nota.
 Artículo relacionado
Artículo relacionado




